Уксусный альдегид: свойства, получение, использование

На данное время известны миллион химических соединений. И многие из них относится к органическим. Эти вещества разделяют на несколько больших групп, наименование одной из них — альдегиды.
Сегодня мы будем рассматривать представителя данного класса — уксусный альдегид.
Обозначение
Уксусный альдегид считается органическим соединением класса альдегидов. Его как правило называют и по-иному: ацетальдегидом, этаналем или метилформальдегидом.
Формула уксусного альдегида — CH3-CHO.

Окисление спирта до альдегида

Как правило уксусный альдегид получают при помощи окисления этена (процесс Вакера). В роли окислителя выступает хлорид палладия. Еще данное вещество можно получить во время гидратации ацетилена, в которой присутствуют соли ртути.
Продуктом реакции считается енол, который изомеризуется в искомое вещество. Очередной способ получения уксусного альдегида, который был самым популярным прежде, как стал известным процесс Вакера, — окисление или дегидратация этанола в наличии медного или серебряного катализаторов.
При дегидратации, кроме искомого вещества, образуется водород, а во время окисления — вода.
При помощи обсуждаемого соединения получают бутадиен, альдегидные полимерные материалы и некоторые органические вещества, в том числе и одноимённую кислоту. Она образуется при его окислении.
Реакция выглядит так: "кислород + уксусный альдегид = кислота уксуса". Этаналь — значимый прекурсор ко многим производным, и данное свойство повсеместно используется в синтезе
многих веществ. В организмах человека, зверей и растений ацетальдегид считается участником некоторых трудных реакций.
Также он входит в состав сигаретного дыма.
Ацетальдегид может приносить как пользу, так и вред. Он пагубно влияет на поверхность кожи, считается ирритантом и, может быть, канцерогеном.
По этой причине его наличие в организме нежелательно. Однако некоторые люди сами провоцируют возникновение ацетальдегида, куря сигареты и потребляя хмельной напиток.
Стоит подумать над этим!
Качественная реакция на альдегиды с гидроксидом меди
Альдегиды, их строение и свойства. Получение, использование муравьиного и уксусного альдегидов.
Альдегиды – это органические соединения, в состав молекулы которых входит карбонильная группа, соединённая с водородом и углеводородным радикалом.
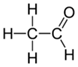
Этаналь
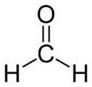
Метаналь (муравьиный альдегид)
Физические свойства
Метаналь – газообразное вещество, раствор воды – формалинь
Химические свойства
Реактивом на альдегиды считается Cu(OH)2
Самое большое использование имеют метаналь и этаналь. Очень много метаналя применяется для получения фенолформальдегидной смолы, которую получают при взаимном действии метаналя с фенолом.
Эта смола нужна для изготовления разных пластмасс. Пластмассы сделаны для из фенолформальдегидной смолы в комбинировании с разными наполнителями, называются фенопластами. При растворении фенолформальдегидной смолы в ацетоне или спирту получают разные лаки.
При взаимном действии метаналя с карбамидом CO(NH2)2 получают карбидную смолу, а из нее – аминопласты. Из данных пластмасс делают микропористые материалы для нужд электробытовой техники.Метаналь идёт также на производство некоторых лекарственных веществ и красителей.
Повсеместно используется раствор воды, который содержит в массовых долях 40% метаналя. Он называетсяформалином.
Его применение основано на свойстве свёртывать белок.
Альдегиды получают окислением алканов и спиртов. Этаналь получают гидротациейэтина и окислением этилена.
Электрохимический ряд стрессов металлов
Li, K, Ca, Na, Mg, Al, Zn, Cr, Fe, Pb, H2, Cu, Ag, Hg, Au
Чем левее стоит металл в ряду типовых электродных потенциалов, тем достаточно сильным восстановителем он считается, самый крепкий восстановитель – железный литий, золото – самый слабый, и, наоборот, ион золото (III) – самый крепкий окислитель, литий (I) – самый слабый.
Каждый металл способен воссоздавать из солей в растворе те металлы, которые стоят в ряду стрессов после него, к примеру, железо может вытеснять медь из растворов ее солей. Но не забывайте, что металлы щелочных и щелочно-земельных металлов будут взаимодействовать конкретно с водой.
Металлы, стоящее в ряду стрессов левее водорода, способны вытеснять его из растворов разбавленных кислот, при этом растворяться в них.
Реставрационная активность металла не всегда отвечает его положению в периодической системе, так как при подсчете места металла в ряду принимается во внимание не только его способность отдавать электроны, но и энергия, которая тратится на разрушение кристаллической решётки металла, и еще энергия, затрачиваемая на гидратацию ионов.
Дата добавки: 2019-07-15 ; просмотров: 262 ;
10.3. Альдегиды и кетоны: Химические свойства. ЕГЭ по химии
Уксусный альдегид

Общая характеристика
Уксусный альдегид имеет пару наименований: ацетальдегид, этаналь, метилформальдегид. Это соединение считается альдегидом уксусной кислоты и этанола.
Его структурная формула выглядит так: CH3-CHO.
Рис. 1. Химическая формула уксусного альдегида.
Спецификой этого альдегида считается то, что он встречается как в природе, так и производится искусственным методом. В промышленности объем изготовления данного вещества может составлять до 1 миллиона тонн в течении года.
Этаналь встречается в пищевых продуктах, например как кофе, хлеб, и еще это вещество синтезируют растения в процессе метаболизма.
Уксусный альдегид собой представляет жидкость без цвета, но отличающуюся резким запахом. Растворим в водной массе, спирте и эфире. считается токсичным.

Изучение свойств уксусной кислоты – OLabs – Университет Амрита.
Жидкость закипает при довольно невысокой температуре – 20,2 градуса по шкале Цельсия. Благодаря этому появляются проблемы с ее хранением и транспортировкой.
По этой причине хранят вещество в виде паральдегида, а ацетальдегид из него получают если необходимо путем нагревания с серной кислотой (либо с любой иной минеральной кислотой). Паральдегид – это циклический тример уксусной кислоты.
Способы получения
Получить уксусный альдегид можно несколькими вариантами. Более простой вариант – окисление этена или, их еще называют такой способ, процесс Вакера:
Окислителем в этой реакции выступает хлорид палладия.
Также уксусный альдегид можно получить пр взаимном действии ацетилена с солями ртути. Эта реакция носит имя русского ученого и именуется реакцией Кучерова. В результате химического процесса образуется енол, который изомеризуется в альдегид
Рис. 3. М. Г. Кучеров портрет.
До открытия метода Вакера в 60-ые годы уксусный альдегид получали с помощью этилового спирта. Этиловый спирт окисляли или дегидрировали. В качестве катализатора выступали медь или серебро:
По химическим особенностям ацетальдегид считается обычным представителем альдегидов.
Используют в промышленности данное вещество для получения уксусной кислоты, бутадиена и самых разнообразных органических веществ.
Что мы узнали?
Уксусный альдегид – жидкость, имеющая несколько наименований. Это вещество имеет особенность кипеть уже при температуре 20,2 градуса.
Есть два главных способа благодаря которым получают этот альдегид: реакция Вакера и реакция Кучерова.

